Περιγραφή
| Εμπορική ονομασία | XOFIGO |
| Κάτοχος άδειας κυκλοφορίας | Bayer Healthcare AG |
| Κατηγορία προϊόντος | Φάρμακα ανθρώπινης χρήσης |
| Κύρια ομάδα ATC |
V10XX03
Radium (223Ra) dichloride
|
| Ομάδες ATC εμπορικής |
V10XX03
Radium (223Ra) dichloride
|
| Φαρμακοτεχνική μορφή | Ενέσιμο διάλυμα (INJ_SOL) |
| Συγκέντρωση | 1000[arb'U]/ML |
| Συσκευασία | 1 BOX * 1 VIAL * 6 ML |
| Οδοί χορήγησης | Ενδοφλέβια (IV) |
| Αριθμός δόσεων | 1 VIAL |
| Λοιπές πληροφορίες |
Διαυγές, άχρωμο ισοτονικό διάλυμα με pH μεταξύ 6,0 και 8,0. |
Αριθμοί αναγνώρισης
2803065201010
• Γαληνός 22746 • Ε.Ο.Φ. 30652.01.01 • Η.ΔΙ.Κ.Α. 10071
Έλεγχος συγχορήγησης
Αναζήτηση αλληλεπιδράσεων μεταξύ ουσιών και νόσων
Προχωρήστε στον έλεγχοΕνεργά συστατικά
|
RJ00KV3VTG - RADIUM RA-223 DICHLORIDE
Το ράδιο-223 (ως διχλωρίδιο του ραδίου-223) μιμείται το ασβέστιο και στοχεύει επιλεκτικά τα οστά, ειδικότερα περιοχές οστικών μεταστάσεων, σχηματίζοντας σύμπλοκα με το μεταλλικό στοιχείο των οστών υδροξυαπατίτη. Η μονοθεραπεία με διχλωρίδιο του ραδίου-223 ή σε συνδυασμό με ανάλογο της ορμόνης απελευθέρωσης της ωχρινοτρόπου ορμόνης (LHRH) ενδείκνυται για τη θεραπεία ενηλίκων ασθενών με μεταστατικό, ανθεκτικό στον ευνουχισμό καρκίνο του προστάτη (mCRPC). |
Συσκευασία και συγκέντρωση
Το σκεύασμα παρουσιάζει τον εξής τρόπο συσκευασίας:
Η συγκέντρωση των δραστικών ουσιών αναλύεται ως εξής:
Η συνολική ποσότητα δραστικών ουσιών ανά σκεύασμα είναι:
Κατάλογος εκδόχων
| Περιγραφή | Κωδικός UNII |
|---|---|
| Κιτρικό νάτριο | 1Q73Q2JULR SODIUM CITRATE, UNSPECIFIED FORM |
| Υδροχλωρικό οξύ, αραιωμένο | QTT17582CB HYDROCHLORIC ACID |
| Ύδωρ για ενέσιμα | 059QF0KO0R WATER |
| Χλωριούχο νάτριο | 451W47IQ8X SODIUM CHLORIDE |
Ποιοτική και ποσοτική σύνθεση
Κάθε mL διαλύματος περιέχει 1100 kBq διχλωριδίου του ραδίου Ra 223 (διχλωρίδιο του ραδίου-223), που αντιστοιχεί σε 0,58 ng ραδίου-223 κατά την ημερομηνία αναφοράς. Το ράδιο είναι παρόν στο διάλυμα ως ελεύθερο ιόν.
Κάθε φιαλίδιο περιέχει 6 mL διαλύματος (6,6 MBq διχλωριδίου του ραδίου-223 κατά την ημερομηνία αναφοράς).
Το ράδιο-223 είναι ένας εκπομπός σωματιδίων άλφα με χρόνο ημιζωής 11,4 ημέρες. Η ειδική ενεργότητα του ραδίου-223 είναι 1,9 MBq/ng.
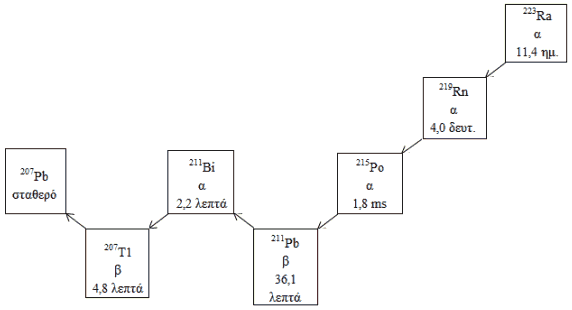
Η διάσπαση έξι σταδίων του ραδίου-223 σε μόλυβδο-207 λαμβάνει χώρα μέσω θυγατρικών μικρής ημιζωής, και συνοδεύεται από έναν αριθμό εκπομπών άλφα, βήτα και γάμμα, με διαφορετικές ενέργειες και πιθανότητες εκπομπής. Το κλάσμα της ενέργειας που εκπέμπεται από το ράδιο-223 και τα θυγατρικά του ως σωματίδια άλφα είναι 95,3% (εύρος ενέργειας 5,0-7,5 MeV). Το κλάσμα που εκπέμπεται ως σωματίδια βήτα είναι 3,6% (οι μέσες ενέργειες είναι 0,445 MeV και 0,492 MeV), και το κλάσμα που εκπέμπεται ως ακτινοβολία γάμμα είναι 1,1% (εύρος ενέργειας 0,01-1,27 MeV).
Εικόνα 1. Αλυσίδα διάσπασης του ραδίου-223 με φυσικές ημιζωές και τρόπο διάσπασης
Έκδοχα με γνωστές δράσεις: Κάθε mL διαλύματος περιέχει 0,194 mmol (που ισοδυναμεί με 4,5 mg) νατρίου.
Για τον πλήρη κατάλογο των εκδόχων, βλ. παράγραφο 6.1.
Σχετικό SPC
Xofigo 1100 kBq/mL ενέσιμο διάλυμα.
Το πηγαίο έγγραφο είναι διαθέσιμο προς ανάγνωση ή μεταφόρτωση από τους συνδρομητές.